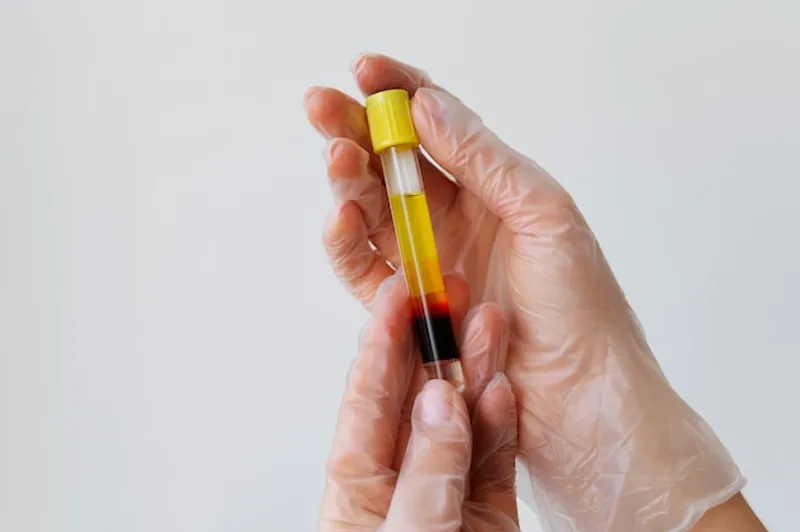
Les facteurs de croissance issus de la FRPC (Fibrine Riche en Plaquettes et Cytokines) représentent une avancée majeure dans la médecine régénérative. Cette technique sophistiquée repose sur des principes scientifiques rigoureux, impliquant l’extraction et la concentration des protéines bioactives naturellement présentes dans le sang du patient. Ces facteurs de croissance jouent un rôle crucial dans la régénération tissulaire, la cicatrisation et la modulation de la réponse inflammatoire, offrant des applications thérapeutiques prometteuses dans divers domaines médicaux.
Introduction aux facteurs de croissance FRPC
Les Facteurs de Croissance Riches en Plaquettes et Cytokines (FRPC) représentent une avancée majeure dans le domaine de la médecine régénérative. Cette technologie biomédical sophistiquée utilise les propres ressources biologiques du patient pour stimuler et accélérer les processus naturels de guérison. Le FRPC est obtenu à partir d’un prélèvement sanguin du patient, qui est ensuite traité selon un protocole spécifique pour isoler et concentrer les facteurs de croissance.
La communauté scientifique a démontré que le FRPC contient une concentration élevée de protéines bioactives et de facteurs de croissance qui jouent un rôle crucial dans la régénération tissulaire. Ces éléments sont naturellement présents dans notre organisme et interviennent dans de nombreux processus biologiques essentiels, notamment la réparation cellulaire, l’angiogenèse et la modulation de l’inflammation.
Définition et composition des facteurs de croissance
D’un point de vue moléculaire, les facteurs de croissance FRPC sont des glycoprotéines hautement spécialisées qui se caractérisent par leur structure complexe. Les principaux composants incluent :
- PDGF (Facteur de Croissance Dérivé des Plaquettes)
- TGF-β (Facteur de Croissance Transformant Bêta)
- IGF (Facteur de Croissance Analogue à l’Insuline)
- VEGF (Facteur de Croissance Endothélial Vasculaire)
La biosynthèse de ces facteurs de croissance s’effectue principalement dans les mégacaryocytes de la moelle osseuse, qui sont les cellules précurseurs des plaquettes. Lors du processus de préparation du FRPC, ces facteurs sont libérés des α-granules plaquettaires à travers un processus d’activation contrôlé.
Les études moléculaires ont révélé que chaque facteur de croissance possède une séquence peptidique unique qui détermine sa spécificité d’action et sa capacité à se lier aux récepteurs cellulaires cibles.
Rôle physiologique dans l’organisme
Dans l’organisme, les facteurs de croissance FRPC exercent des fonctions biologiques essentielles à travers différents mécanismes d’action. Ils agissent comme des messagers moléculaires qui coordonnent la réparation tissulaire et la régénération cellulaire.
Les principaux rôles physiologiques comprennent :
- Stimulation de la prolifération cellulaire
- Promotion de l’angiogenèse
- Modulation de la réponse inflammatoire
- Activation des cellules souches
La cascade de signalisation initiée par ces facteurs de croissance implique une communication intercellulaire complexe, aboutissant à l’activation de voies métaboliques spécifiques qui favorisent la régénération tissulaire. Les études cliniques ont démontré leur efficacité particulière dans l’accélération des processus de cicatrisation et la réduction des temps de récupération post-opératoires.
Pour approfondir vos connaissances sur les applications thérapeutiques des facteurs de croissance FRPC, nous vous invitons à consulter nos autres articles détaillant leur utilisation en chirurgie dentaire, en médecine sportive et en dermatologie esthétique.
Mécanismes d’action moléculaires
Les facteurs de croissance PRGF (Plasma Rich in Growth Factors) représentent une avancée significative dans la médecine régénérative. Leur mécanisme d’action repose sur une série d’interactions moléculaires complexes qui stimulent la régénération tissulaire. Ces protéines bioactives agissent comme des messagers cellulaires qui orchestrent la réparation et la régénération des tissus endommagés.
La spécificité de leur action est déterminée par leur structure moléculaire unique, qui leur permet de se lier à des récepteurs cellulaires spécifiques. Les principaux facteurs de croissance présents dans le PRGF incluent :
- Le PDGF (Platelet-Derived Growth Factor)
- Le TGF-β (Transforming Growth Factor Beta)
- Le VEGF (Vascular Endothelial Growth Factor)
- L’IGF-1 (Insulin-like Growth Factor 1)
Interaction avec les récepteurs cellulaires
L’interaction entre les facteurs de croissance et leurs récepteurs cellulaires suit un processus hautement régulé. Lorsqu’un facteur de croissance se lie à son récepteur spécifique sur la membrane cellulaire, il se produit une modification conformationnelle du récepteur, déclenchant une cascade de signalisation intracellulaire.
Cette liaison spécifique active des récepteurs tyrosine kinase qui s’autophosphorylent, créant des sites d’ancrage pour les protéines de signalisation intracellulaire. Ce processus est crucial pour la transmission du signal et la régulation des fonctions cellulaires.
La spécificité de ces interactions est renforcée par la présence de corécepteurs et de molécules adaptatrices qui modulent la réponse cellulaire. Cette complexité permet une régulation fine des processus de régénération tissulaire.
Cascades de signalisation intracellulaire
Une fois les récepteurs activés, plusieurs voies de signalisation majeures sont mises en jeu. Les principales cascades comprennent :
- La voie MAP kinase (MAPK)
- La voie PI3K/AKT
- La voie JAK/STAT
Ces cascades de signalisation conduisent à l’activation de facteurs de transcription spécifiques qui régulent l’expression des gènes impliqués dans la prolifération cellulaire, la différenciation et la survie. La coordination de ces voies permet une réponse cellulaire optimale et contrôlée. Les études récentes ont démontré que la synchronisation temporelle de ces cascades de signalisation est cruciale pour obtenir une réponse thérapeutique optimale. La compréhension de ces mécanismes permet d’optimiser les protocoles de traitement PRGF.
Pour approfondir vos connaissances sur les applications cliniques des facteurs de croissance et leurs effets thérapeutiques, nous vous invitons à consulter nos autres articles détaillés sur la régénération tissulaire et les protocoles de traitement PRGF.
Processus de concentration et d’activation
Le Plasma Riche en Facteurs de Croissance (PRGF) nécessite un protocole précis pour garantir son efficacité thérapeutique. La concentration et l’activation des facteurs de croissance représentent les étapes cruciales du processus, déterminant directement la qualité du traitement. Les études récentes démontrent qu’une concentration optimale se situe entre 2 à 3 fois le niveau basal des plaquettes.
La manipulation du PRGF doit être réalisée dans des conditions strictement contrôlées pour maintenir la stabilité des protéines bioactives. La température, le pH et le temps de manipulation sont des paramètres essentiels qui influencent directement la qualité du produit final. Les recherches menées par l’équipe du Dr. Anitua ont établi que la température idéale de manipulation se situe entre 21°C et 24°C.
Techniques de concentration
La centrifugation constitue l’étape fondamentale du processus de concentration. Elle s’effectue selon des paramètres précis : une vitesse de rotation comprise entre 1800 et 2200 RPM pendant 8 minutes, permettant une séparation optimale des différentes fractions sanguines.
Le processus de concentration implique plusieurs étapes critiques :
- Prélèvement sanguin dans des tubes citratés spécifiques
- Centrifugation à température contrôlée
- Séparation méticuleuse des fractions plasmatiques
- Isolation de la fraction riche en facteurs de croissance
La qualité de la concentration dépend également de la précision du pipetage, qui doit être réalisé par un personnel qualifié. Les études montrent qu’une technique rigoureuse permet d’obtenir une concentration en facteurs de croissance jusqu’à 3 fois supérieure aux valeurs basales.
Activation et stabilisation
L’activation des facteurs de croissance s’effectue principalement par l’ajout de chlorure de calcium, déclenchant la cascade de coagulation et la libération des protéines bioactives. Ce processus doit être minutieusement contrôlé pour garantir une activation optimale sans dénaturation des protéines.
La stabilisation du PRGF activé nécessite des conditions particulières :
- Maintien d’une température constante
- Protection contre la lumière UV
- Utilisation de contenants stériles appropriés
- Respect des délais d’utilisation
La durée de vie des facteurs de croissance activés est limitée, généralement entre 4 et 6 heures après l’activation. Les recherches actuelles travaillent sur des méthodes de stabilisation permettant de prolonger cette durée tout en préservant l’efficacité thérapeutique.
Pour approfondir vos connaissances sur les applications cliniques du PRGF et découvrir les dernières avancées dans ce domaine, nous vous invitons à consulter nos autres articles sur la régénération tissulaire et les protocoles thérapeutiques innovants.
Applications thérapeutiques
Le Plasma Riche en Facteurs de Croissance (FRPC) représente une avancée majeure dans la médecine régénérative moderne. Cette technologie innovante exploite les propriétés naturelles de guérison du corps en concentrant les facteurs de croissance présents dans le plasma sanguin. Les applications thérapeutiques du FRPC sont particulièrement vastes, allant de la chirurgie dentaire à la médecine sportive.
L’efficacité du FRPC repose sur sa capacité à stimuler les mécanismes naturels de réparation tissulaire. Les études cliniques ont démontré que les facteurs de croissance présents dans le FRPC peuvent accélérer jusqu’à 30% le processus de cicatrisation par rapport aux méthodes traditionnelles. Cette technique présente l’avantage majeur d’être totalement autologue, utilisant le propre sang du patient, ce qui élimine tout risque de rejet ou de transmission de maladies.
Régénération tissulaire
La régénération tissulaire assistée par FRPC s’appuie sur l’action combinée de plusieurs facteurs de croissance essentiels. Les principaux acteurs sont le PDGF (Platelet-Derived Growth Factor) et le TGF-β (Transforming Growth Factor Beta), qui jouent un rôle crucial dans la stimulation de la prolifération cellulaire et la formation de nouveaux vaisseaux sanguins.
Les applications en régénération tissulaire concernent principalement :
- La régénération osseuse en implantologie dentaire
- La réparation des tissus mous en chirurgie plastique
- La régénération du cartilage articulaire
- La revitalisation des tissus cutanés
Les recherches récentes ont démontré que l’utilisation du FRPC peut augmenter la densité osseuse jusqu’à 40% dans les cas de greffes osseuses, offrant ainsi des résultats particulièrement prometteurs en implantologie dentaire.
Cicatrisation et réparation
Le processus de cicatrisation assisté par FRPC se caractérise par une cascade d’événements biologiques précisément orchestrés. Les facteurs de croissance libérés par les plaquettes activées stimulent la migration des cellules réparatrices et accélèrent la formation de nouveau tissu conjonctif. Les études cliniques ont identifié plusieurs phases clés dans le processus de réparation :
- Phase inflammatoire initiale optimisée
- Stimulation de l’angiogenèse
- Production accrue de collagène
- Remodelage tissulaire amélioré
L’efficacité du FRPC dans la cicatrisation a été particulièrement documentée dans le traitement des plaies chroniques et des lésions musculo-tendineuses, avec des taux de succès atteignant 85% dans certaines études cliniques.
Si vous souhaitez approfondir vos connaissances sur les thérapies régénératives avancées, nous vous invitons à consulter nos autres articles détaillés sur les innovations en médecine régénérative et les dernières avancées en matière de traitement par facteurs de croissance.
Avancées et perspectives futures
Les facteurs de croissance PRGF ont connu des avancées significatives ces dernières années, révolutionnant plusieurs domaines de la médecine régénérative. Les recherches récentes démontrent une efficacité accrue dans la régénération tissulaire, notamment en chirurgie orale et maxillo-faciale.
Les études cliniques menées dans des centres de recherche internationaux ont mis en évidence une amélioration notable des protocoles d’extraction et de préparation. La standardisation des procédures a permis d’obtenir des résultats plus prévisibles et reproductibles, ouvrant la voie à une utilisation plus large en pratique clinique.
Innovations récentes
L’une des innovations majeures concerne l’optimisation de la concentration plaquettaire dans les préparations PRGF. Les nouvelles techniques de centrifugation permettent désormais d’obtenir des concentrations plus précises et adaptées à chaque application spécifique.
Les chercheurs ont également développé de nouveaux systèmes de libération contrôlée des facteurs de croissance, permettant une action plus ciblée et prolongée. Ces avancées ont notamment permis d’améliorer:
- La régénération osseuse en implantologie
- La cicatrisation des tissus mous
- Le traitement des lésions parodontales
- La revascularisation des tissus
La combinaison du PRGF avec des biomatériaux de nouvelle génération a démontré des résultats prometteurs, notamment dans le domaine de la régénération osseuse guidée.
Directions futures de recherche
Les perspectives de recherche s’orientent vers plusieurs axes prometteurs. L’un des domaines les plus encourageants concerne l’utilisation du PRGF dans le traitement des pathologies neurodégénératives, où des études préliminaires montrent des résultats intéressants.
Les chercheurs explorent également l’intégration de technologies d’intelligence artificielle pour optimiser la préparation et l’application du PRGF. Ces avancées pourraient permettre une personnalisation plus précise des traitements en fonction des caractéristiques biologiques de chaque patient.
Les directions futures incluent notamment:
- Le développement de formulations à libération prolongée
- L’exploration de nouvelles applications thérapeutiques
- L’amélioration des techniques de conservation
- L’optimisation des protocoles cliniques
Pour approfondir vos connaissances sur les facteurs de croissance PRGF et leurs applications cliniques, nous vous invitons à consulter nos autres articles détaillés sur les protocoles spécifiques et les cas cliniques documentés.
Questions fréquentes sur les principes scientifiques de la PRGF
Découvrez les réponses aux questions les plus courantes concernant les facteurs de croissance PRGF (Plasma Riche en Facteurs de Croissance) et leurs principes scientifiques fondamentaux.
Qu’est-ce que la PRGF et comment fonctionne-t-elle ?
La PRGF est une technique qui utilise le plasma sanguin du patient, enrichi en facteurs de croissance. Ces protéines naturelles stimulent la régénération tissulaire et accélèrent la cicatrisation. Le processus implique le prélèvement d’un échantillon sanguin qui est ensuite centrifugé pour isoler les facteurs de croissance.
Quels sont les principaux facteurs de croissance présents dans la PRGF ?
Les principaux facteurs comprennent le PDGF (facteur de croissance dérivé des plaquettes), le TGF-β (facteur de croissance transformant bêta), et le VEGF (facteur de croissance endothélial vasculaire). Chacun joue un rôle spécifique dans la régénération tissulaire.
Quels sont les avantages scientifiquement prouvés de la PRGF ?
Les études cliniques ont démontré que la PRGF accélère la cicatrisation, réduit l’inflammation, stimule la formation osseuse et améliore la régénération des tissus mous. Cette technique est particulièrement efficace en chirurgie dentaire et en médecine régénérative.